|
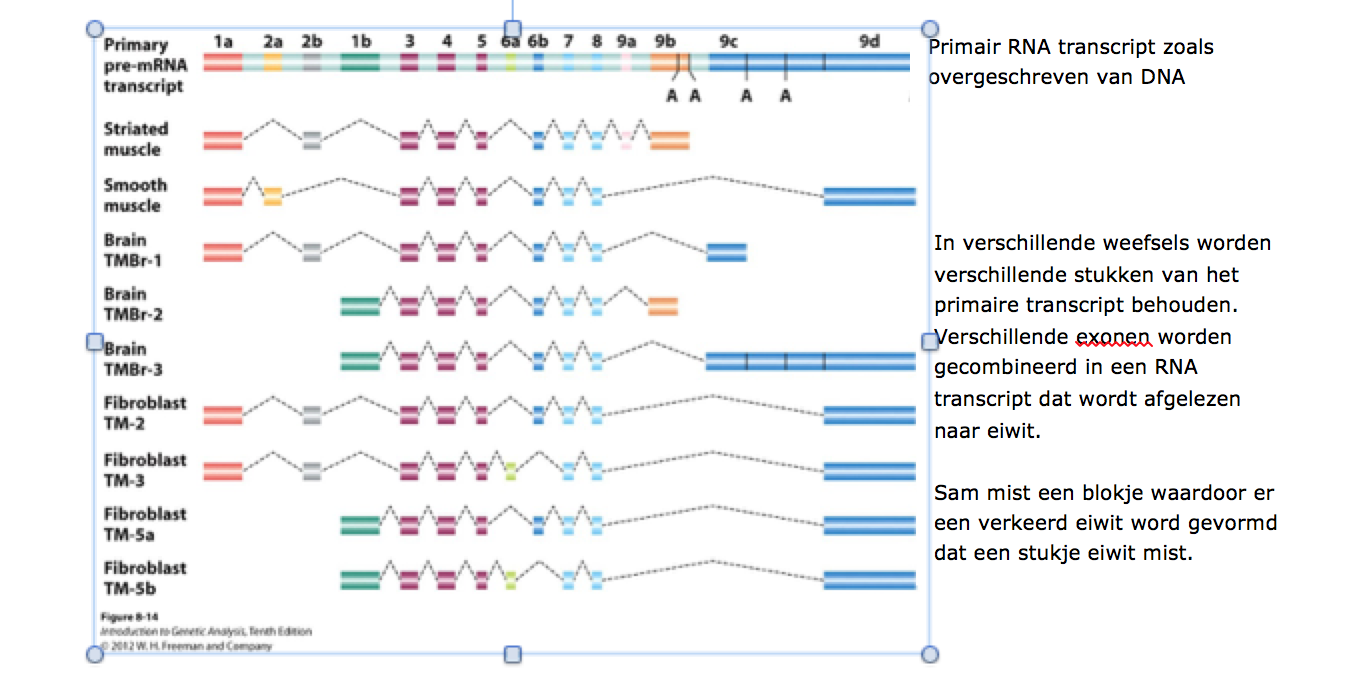
Het syndroom van Marfan is een aangeboren genetische aandoening, veroorzaakt door een ‘foutje’ in het DNA. Door een mutatie in het DNA van Sam, specifiek het FBN1 gen, wordt zijn bindweefsel niet goed aangemaakt. Neonatale Marfan is weer een mutatie van het normale Marfansyndroom, en zit op een ander stukje DNA. Hoe dat precies allemaal werkt is vrij ingewikkeld. Onze zwager Siemen, die werkzaam is als Universitair docent Genetica bij de Universiteit van Wageningen, heeft geprobeerd het ons in ‘normale mensentaal’ uit te leggen. Ons lichaam bestaat uit vele eiwitten, deze eiwitten zijn zowel bouwstenen als enzymen die bepaalde acties en metabolisme van het lichaam mogelijk maken. De genetische informatie voor deze eiwitten zit in ons DNA. Binnen het DNA is een gen een functioneel stuk, we hebben ongeveer 30.000 genen. Naast genen die coderen voor eiwitten ligt er nog veel meer informatie op ons DNA, bijvoorbeeld regio’s voor regulatie welke genen er aan of uit staan. DNA wordt eerst afgelezen in de kern van de cel, tijdens het aflezen wordt DNA gekopieerd naar RNA dat lijkt op DNA. Dit RNA wordt uit de kern getransporteerd naar speciale cel fabriekjes (ribosomen) waar het RNA wordt afgelezen en er eiwitten worden gemaakt. Eiwitten op hun beurt bestaan uit bouwstenen die we aminozuren noemen. Er zijn 20 verschillende aminozuren waaruit dus alle eiwitten zijn opgebouwd. Er zijn veel meer verschillende eiwitten dan er genen zijn, ongeveer 1 miljoen eiwitten en maar 30.000 genen. We weten nu dat 1 gen voor meerdere eiwitten kan coderen en wel op de volgende manier. Uit een RNA transcript van DNA worden stukken geknipt die niet worden afgelezen bij het maken van eiwit. Overgebleven stukken RNA worden aan elkaar gezet en dit verwerkte RNA wordt afgelezen naar eiwit. De stukken die eruit geknipt worden heten intronen, de stukken die bij elkaar worden gecombineerd en naar eiwit worden overgeschreven heten exonen. Het eruit knippen wordt splicing genoemd en het knippen gebeurt op splicing sites. Eén origineel RNA transcript kan op verschillende manieren worden bewerkt, de stukken die eruit geknipt worden (de intronen) en de stukken die overblijven (exonen) zijn niet steeds hetzelfde. Zo kan één primair transcript voor een groot aantal verschillende eiwitten coderen. De figuur hieronder laat dit zien. Bij het Marfan syndroom gaat er iets mis met het verwerken van het primaire RNA transcript dat vanuit het DNA is gevormd. Het FBN1-gen is verantwoordelijk voor een eiwit dat belangrijk is bij bindweefsel. Het verwerkte RNA dat overgeschreven wordt naar eiwit bevat 65 exonen, dus 65 gekleurde blokjes als getekend in de figuur. Er kunnen mutaties in het DNA zitten die zorgen dat het uitknippen van intronen en bij elkaar zetten van exonen niet goed verloopt. Uit een studie is bekend dat neonatale Marfan mutaties op het DNA heeft die zorgen dat exonen ergens tussen exon nummer 24 en 30 niet goed worden gecombineerd.
In het dossier van Sam staat dat hij een mutatie heeft in een splice site (knipplek in het primaire RNA waar dus intronen worden uitgeknipt en exonen worden behouden). Dit is mutatie c.3338-1G>A op het gen FBN1 (op plek c.3338 staat er geen G maar een A op het DNA). Gevolg is dat er niet goed wordt gecombineerd en dat Sam 1 exon mist (exon #27 of #28 afhankelijk van de telling). Hierdoor mist Sam in het uiteindelijke eiwit dat belangrijk is voor bindweefsel 42 bouwstenen (aminozuren). Er is een wetenschappelijk artikel waarbij gekeken is naar patiënten die een exon missen ergens tussen exon #24 en #32. Er blijken behoorlijke verschillen in hoe erg de aandoening is en hoe lang de levensverwachting is. Van de 5 patiënten die zijn onderzocht is er 1 inmiddels ouder dan 10 en in leven (mist exon 26), 1 is 8 jaar oud (mist exon 29) en de andere 3 zijn voor hun eerste verjaardag overleden (missen respectievelijk exon 26, 29 en 30). Apart dus dat het missen van exon 26 of 29 hele verschillende gevolgen kan hebben. De studie gaf ook een overzicht van andere studies waar gekeken is naar patienten die ouder zijn geworden dan 2 jaar (niet hoe oud ze uiteindelijk zijn geworden), wat de mutatie op het DNA was en welk exon ontbrak tussen exon 24 en 32. Hier komen ook patienten voor die net als Sam exon 27 of 28 niet hebben. Deze patienten die exon 27 en 28 missen hebben wel andere mutaties op het DNA dan Sam. Een duidelijke conclusie voor wat te verwachten bij Sam is niet gemakkelijk te trekken, ook niet over zijn levensverwachting.
1 Comment
Nancy winklaar
7/6/2021 11:14:58 am
Heel veel sterkte ik bid voor jullie
Reply
Leave a Reply. |
AuteurLaurens en Dessie, de ouders van Sam Archieven
Juni 2022
Categorieën |
 RSS-feed
RSS-feed
